5/7 化学课 - 影响化学平衡移动的因素
化学平衡的移动
概念:可逆发硬中旧化学平衡破坏、新化学平衡建立的过程叫做化学平衡的移动
浓度对化学平衡移动的影响

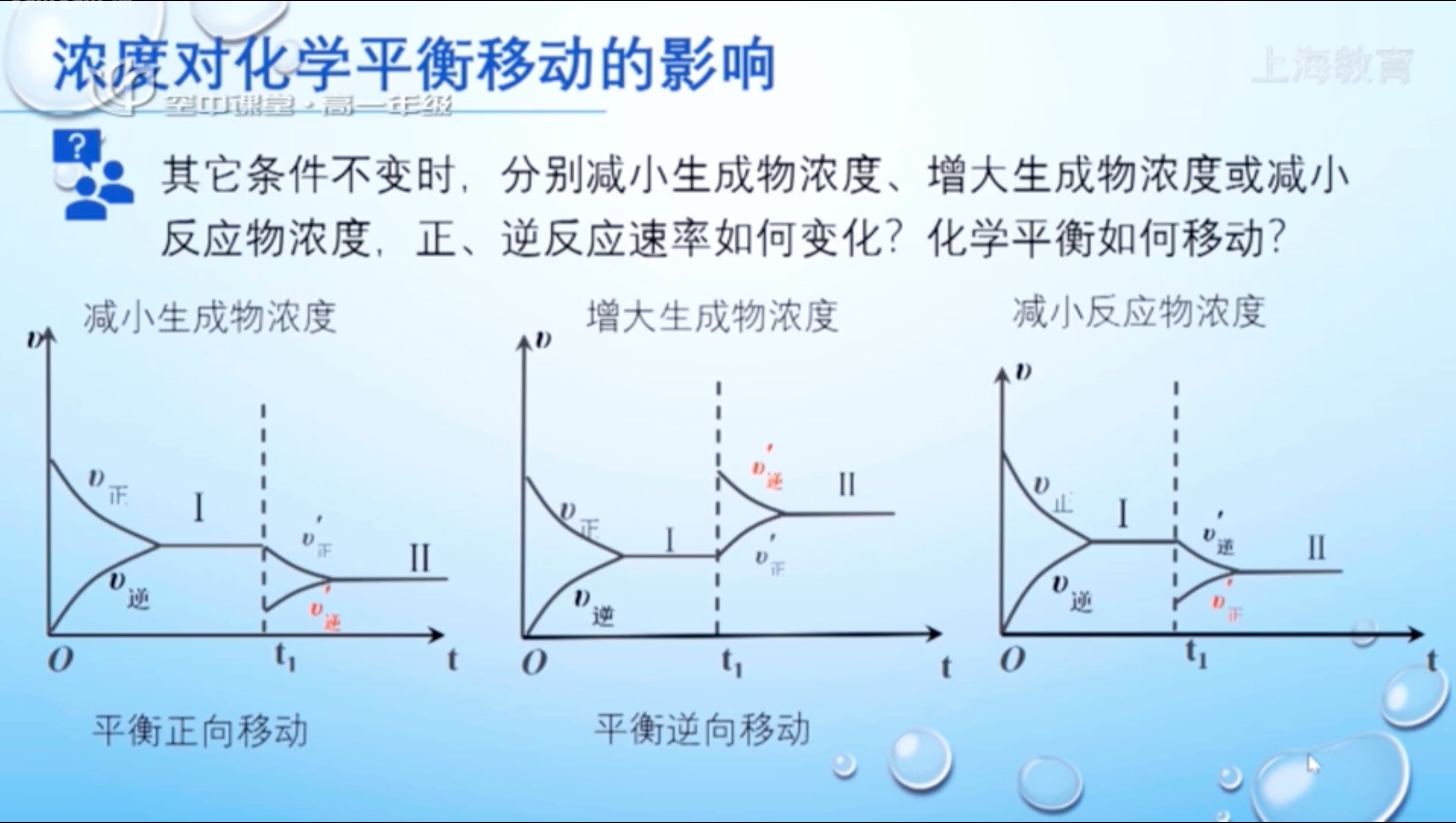
必须是液体或气体
压强对化学平衡移动的影响

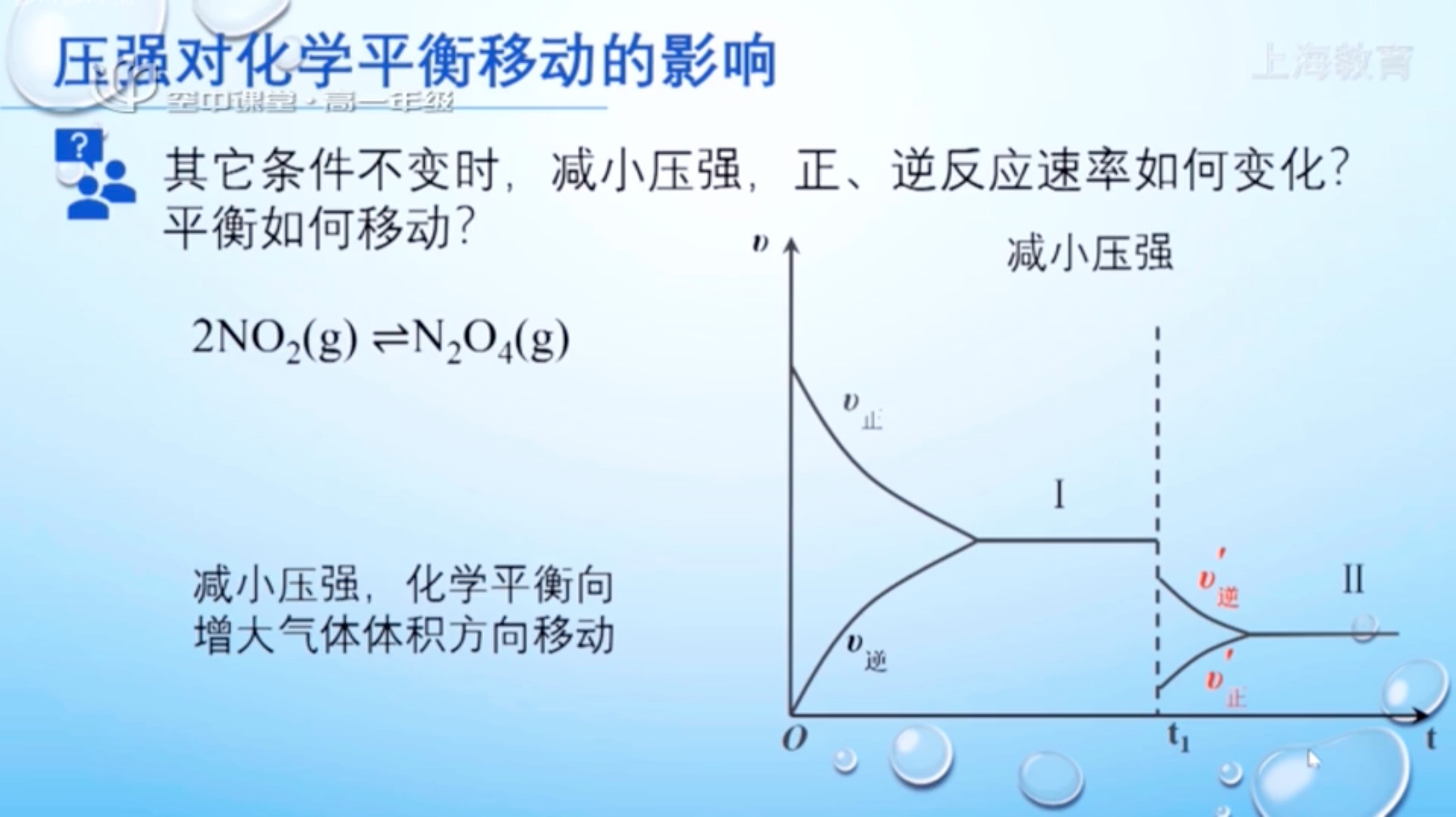
如果平衡混合物都是固体或液体,改变压强也不能是化学平衡发生移动。
温度对化学平衡移动的影响
结论:
- 温度对化学平衡的影响与化学反应的热效应有关。
- 在其他条件不变时,升高温度,化学平衡 向吸热方向移动
- 在其他条件不变时,降低温度,化学平衡 向放热方向移动
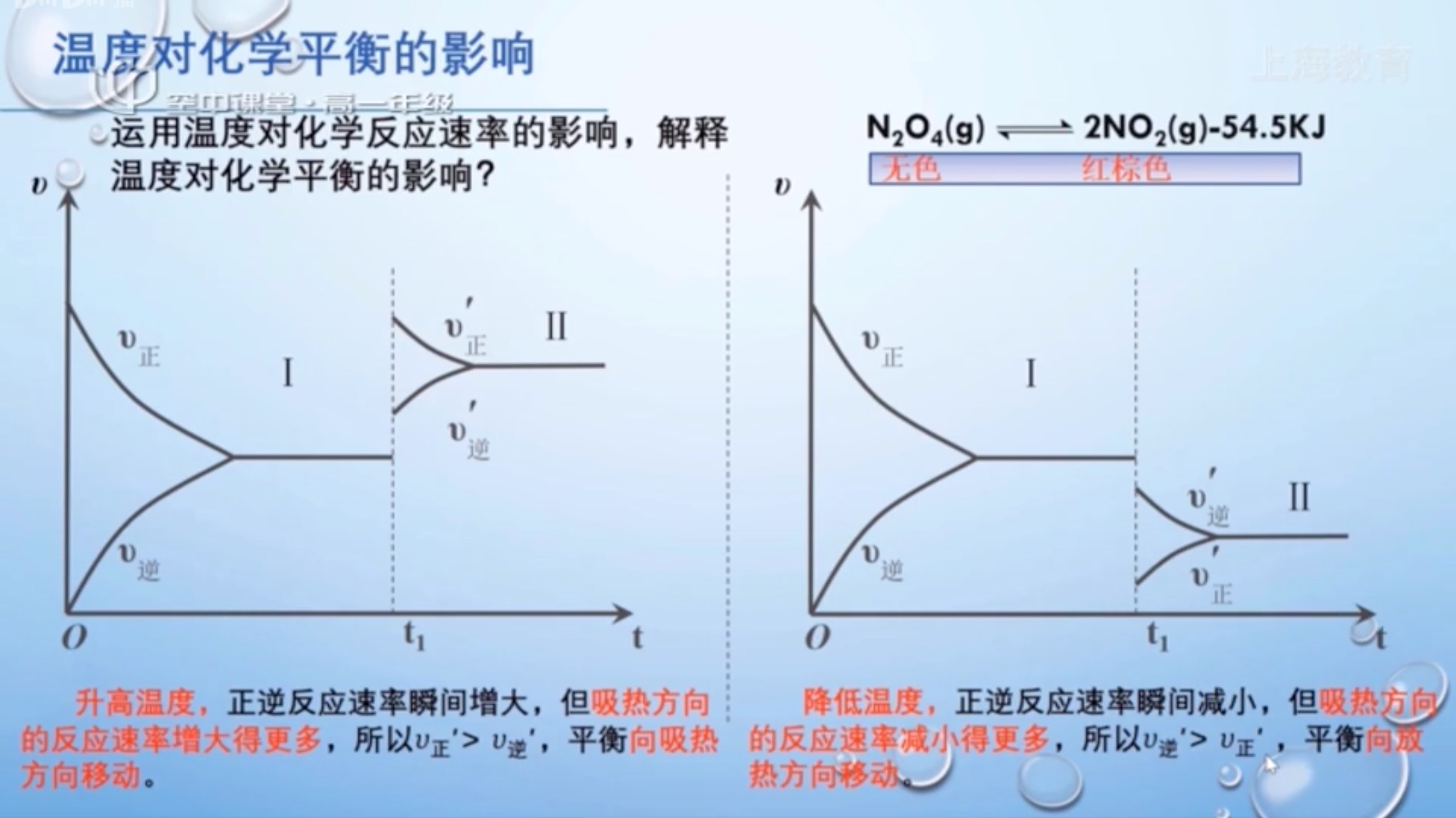
温度对吸热反应方向影响比较大
催化剂对化学平衡的影响
化学平衡不能使化学平衡发生移动
但是催化剂能够大大缩短化学反应的时间
关于充入气体的讨论
我们考察以下反应:
- T、V不变,充入$\ce {N2}$,反应物浓度增加,正反应速率增加,逆反应速率随之增加,反应朝正反应方向移动
- T、V不变,充入$\ce {He}$,反应物浓度不变,正反应速率不变,逆反应速率也不变,化学平衡不移动
- T、P不变,充入$\ce {He}$,压强降低,正逆反应速率均减小,平衡朝增加压强的方向移动,即朝逆反应方向移动注:这里勒沙特列原理不能解释根据勒沙特列原理,充入氮气,会使得氮气的转化率降低,氢气的转化率升高。这个原理广泛应用于工业生产当中。

